嗜粘卵白-阿克曼氏菌(Akkermansia muciniphila,A.muciniphila),简称为 AKK,于 2004 年发现,是一种从人类粪便平分离出来的卵形革兰氏阴性细菌。
该细菌以荷兰微生物生态学家 Anton DL Akkermans 的名字定名,以表扬他对该范畴的奉献。A. muciniphila 是人类肠道共生菌,并能够依靠肠粘液层的黏卵白保存。
在过去十年中,越来越多的研究证明,在糖尿病、心血管疾病、疾病性肠病、神经疾病发现A. muciniphila品貌降低。比来的干涉研究还证明如茶或富含多酚生果的饮食可增加其品貌,有助于改善糖尿病和瘦削个别的代谢功用。
总的来说,来主动物和人类研究的越来越多的证据表白A. muciniphila将成为下一代有临床应用前景的益生菌。尤其是它在预防和治疗糖尿病、瘦削症及癌症,那对将来的研究具有重要意义和开展。
01
什么是 Akkermansia muciniphilaA. muciniphila是一种厌氧、革兰氏阴性、无运动、没有内生胞子的卵圆形肠道细菌,其最适生长温度是37℃,最适生长pH为6.5,该菌的倍增时间大约是1.5 h。A. muciniphila属于疣微菌门,事实上,它是人类粪便样本中发现的属于那个特殊门的独一物种。
值得留意的是,A. muciniphila具有必然的耐氧性,其表露在空气中24 h,仍然有1%以上的存活率。此外,研究还发现低氧气浓度(纳摩尔)下能够显著促进A. muciniphila的生长。
A. muciniphila零丁或者成对存在,很少成链生长,其代谢产品为乙酸盐、丙酸盐、1,2-丙二醇等。
在供给卵白源的根底培育基中,参加N-乙酰氨基葡萄糖、N-乙酰半乳糖胺和葡萄糖做为能源,A. muciniphila能够生长,但是在果糖和纤维二糖等其他糖类做为能源的培育基中A. muciniphila不克不及生长,申明该菌的生长繁衍需要卵白量。
A. muciniphila的出格有趣之处在于,与大大都其他有益细菌差别,它不完全依赖于我们的饮食来喂养。即便消化道中没有营养物量,它也会以粘膜层中的粘卵白为食。
Akkermansia Muciniphila一般通过母体获得, 凡是在儿童中大量存在,并跟着年龄和疾病而削减。将其恢复到更佳程度能够带来许多益处。
肠道中低浓度的Akkermansia muciniphila可能表白黏液层较薄,从而招致肠道屏障功用削弱,此外还会增加细菌毒素的易位,炎症性肠病、哮喘、瘦削症和 II 型糖尿病患者的Akkermansia muciniphila浓度往往较低。
我们晓得整个胃肠道 (GI) 的粘膜完好性关于维持人体安康至关重要。那此中,粘液屏障的完好性是胃肠道的第一道防线。肠道黏液层的周转包罗黏液的合成、排泄和降解,那是一个需要调理和平衡的微妙过程,以确保黏液连结更佳的庇护功用。
粘液由多种成分构成:水 (90%–95%)、电解量、脂量 (1%–2%)、卵白量等。那种粘液是一种稀的、水性和粘弹性的排泄物,那要归功于被称为粘卵白的特定粘液卵白,它是粘液中存在的次要构造和功用成分,浓度为 1%–5%。
粘卵白是一个大的、复杂的、糖基化的卵白量家族,其特征是一个重要的元素,即“粘卵白构造域”。它由一个卵白量核心构成,该核心由含有氨基酸残基脯氨酸 (Pro)、苏氨酸 (Thr) 和丝氨酸 (Ser) 的序列构成,称为富含 PTS 的序列,凡是串联反复,此中 Ser 和 Thr 普遍为 O-糖基化并付与“瓶刷”状构象。
MUC2(黏糖卵白2)的化学构造和肠道粘液的合成
Paone P & Cani PD. Gut. 2020肠道菌群在肠道中的散布梯度随其位置差别而变革;微生物密度从近端到远端肠道增加,每克肠道内容物的微生物细胞数量大约如下:
十二指肠中10^3 个
空肠中 10^4 个
回肠中 10^7个
结肠中10^12 个
此外,微生物密度从上皮细胞向管腔增加,在后者中发现的细菌数量最多,与管腔比拟,现实上很少有细菌物种可以很好地粘拥护驻留在粘液层中。除了粘附那一重要功用外,肠道微生物群对调理肠道粘液层有很大奉献。
需要普及一个认知就是,当我们谈到构成微生物组的各类细菌物种时,有些菌似乎比其他细菌具有更显着的影响,好比肠道基石菌,核心菌,益生菌等,确保那些个别物种的更佳程度——不要太低,也不要太高——能够产生对安康深远的影响。那此中包罗有益细菌的关键物种之一 Akkermansia Muciniphila。
谷禾肠道样本大数据库显示A. muciniphila缺乏或未检出情况在人群中很常见,尤其是那些有肠道问题的人。在安康个别中其约占肠道微生物群总数的0.5%–3%。
但是也有破例,在我们在比来的检测的一个56岁密斯肠道内该菌的品貌占比超50%,菌群构成如下:
然而,功德太多也可能是坏事。它的名字——“muciniphila”的意思是粘液喜好者,指的是它奇特的才能,降解黏卵白和粘液层。过量的Akkermansia 将过度消耗粘液卵白而存活下来,那是大大都其他细菌所缺乏的保存优势。在那种情况下,非粘液消耗物种的数量显着削减,招致物种多样性削减, Akkermansia 增殖异常,从而可能招致肠道屏障损伤,诱发肠道炎症、LPS 进入血液的增加、本身免疫性疾病有关,神经退行性疾病等。
该样本检测陈述也显示菌群多样性低,肠炎和几项慢病留意风险:
此外,在其它研究文献中也得出Akkermansia muciniphila品貌高的负面研究,如:
在中国人中,A. muciniphila菌的品貌与2型糖尿病呈正相关。
血红素在肠道中的过度增生,与A. muciniphila的粘膜消融活性有关,在特定情况中,A. muciniphila参与促进代谢综合征。
北京协和团队发现Akkermansia muciniphila可能参与了系统性红斑狼疮的发作开展,致本身免疫亢进特征。
02
Akkermansia muciniphila的基因组构造通细致菌16S rRNA测序表白其属于疣微菌门(Verrucomicrobia),与Verrucomicrobium spinosum有92%序列类似性,是如今独一已知的人类肠道疣微菌门成员。此中文译名尚无同一,在文献中以阿克曼黏细菌、艾克曼黏细菌等名字呈现。
为了提醒A. muciniphila的功用潜力,对其基因组停止了测序和正文。发现Akkermansia muciniphila在其相对较小的基因组中编码了大量黏卵白降解酶,黏卵白被其降解后其下流聚糖副产品能够穿插饲养其他肠道细菌。
按照DNA-DNA杂交(Digital DNA-DNA hybridiztion,dDDH)将23个Akkermansia属的菌株分为4种,别离为:
Akkermansia sp.CAG
Akkermansia sp.KLE
Akkermansia. muciniphila
Akkermansia. glycaniphila
但是发现它包罗许多候选粘卵白酶编码基因,但缺乏编码典型粘液连系域的基因。
种内存在多样性。在整个基因组中发现的大量噬菌体相关序列,表白病毒在该物种的进化中阐扬了重要感化。此外,挖掘了 37 个胃肠道宏基因组中,确定Akkermansia序列的存在和遗传多样性。在 37 个中,11 个包罗 16S 核糖体 RNA 基因序列,与A. muciniphila 的不异 > 95% , 称为Akkermansia-like 微生物。
瓦赫宁根大学微生物尝试室从蟒蛇体内别离培育出于A. muciniphila 基因序列具有94.4%类似度的新菌株,而且发现它们也具有类似的特征,将该微生物定名为Akkermansia glycaniphila。
03
Akkermansia muciniphila为什么很重要?Akkermansia muciniphila是一种肠道中的黏卵白降解细菌。粘卵白是肠上皮黏液层的重要构成部门。粘卵白由杯状细胞产生肠上皮,是高度糖基化的分子,还包罗丝氨酸、苏氨酸和半胱氨酸,它们在肠组织外表构成通明的粘液层,是大量肠道微生物栖息的次要部位。
A. muciniphila次要定植在胃肠道的外黏液层,以胃肠道的黏卵白做为本身生长的碳和氮来源,其消耗黏卵白与杯状细胞再生黏卵白可以到达动态平衡,从而维持黏液层不变。A.muciniphila以及其排泄物,如囊泡(Extracellular vesicles, EV)通过与结肠上皮细胞Toll受体(Toll-like receptor,TLR)连系及调理慎密毗连卵白的表达等来维持肠道稳态,从而改善高脂饮食诱导的瘦削和炎症性肠病等疾病。
此外,粘卵白还笼盖在呼吸道、消化道和泌尿生殖道的细胞外表。许多癌症(胰腺癌、肺癌、乳腺癌、卵巢癌、结肠癌和其他组织)城市增加粘卵白的产生。粘卵白也在肺部疾病中过度表达,例如哮喘、收气管炎、慢性阻塞性肺病 (COPD) 或囊性纤维化。
Akkermansia muciniphila 高度适应从粘卵白降解中保存——例如,它需要苏氨酸才气生长,而且具有多种合适操纵粘卵白寡糖中的特殊糖类的酶,如唾液酸酶和岩藻糖苷酶,以至硫酸酯酶。表白宿主动物和AKK菌之间的配合进化进入了高级阶段,并表示了那些疣状微生物对宿主的潜在功用意义。因为其向其他细菌物种供给粘卵白降解产品,该物种也是肠道重要的共生菌属。
Akkermansia muciniphila 可以利用粘卵白做为碳、氮和能量的独一来源。虽然宿主肠道层中的许多黏液降解微生物可能具有致病性,但A. muciniphila纷歧样。Akkermansia muciniphila从粘卵白发酵中产生乙酸盐、丙酸盐和乙醇,以调理宿主的生物学功用,包罗宿主免疫反响和脂量代谢。因为A. muciniphila保留在外黏膜层而且不会渗入到内层,因而它的定植是有益的,因为细菌会促进外黏卵白层的天然更新。
04
Akkermansia muciniphila的安康特征除了基因序列多样性外,那种细菌还表示出多种生物学功用,包罗:
促进肠道屏障完好性;
调理免疫反响;
按捺炎症;
穿插喂养他微生物群;
降低某些心脏病风险,如胰岛素抵御、总血胆固醇和脂肪组织贮存;
避免体重增加。
DOI: (10.1111/jam.14911)促进肠道屏障
肠道屏障是一个多层复杂的系统,它允许营养吸收,同时避免微生物及其产品的易位。肠道屏障的毁坏招致管腔内容物进入血流,激活免疫反响并诱发炎症。
粘液笼盖外肠上皮细胞层,起到物理庇护感化,避免微生物和有害化合物的渗入。除了降解粘卵白外,A. muciniphila还被发现能够刺激粘卵白的产生 。
A. muciniphila在避免人类肠道致病菌增殖中的感化
Kalia VC, et al., Indian J Microbiol. 2021本年颁发在Gut Microbes研究得出,固然A. muciniphila 是一种粘卵白降解细菌,但是通过促进排泄型 IEC 的分化,反而增加了粘液的产生。A. muciniphila处置以 Gpr41/43 依赖性体例加强了ISC 增殖,加速肠上皮再生,促进 IEC 发育并维持肠道稳态。
正文:哺乳动物肠上皮细胞(IEC)更新较快,每 3-5 天弥补一次。所有类型的 IEC 都源自肠干细胞(ISC)
粘卵白的周转率为 6-12 小时,内层的周转率约为 1 小时,据信其排泄受神经、激素和旁排泄感化的调理。
在动物模子中,A. muciniphila弥补剂使结肠粘液层的厚度增加了大约 3 倍,明显高于由有益细菌动物乳杆菌引起的厚度增加。此外,在体外,发现A. muciniphila通过间接与肠细胞连系来改善肠细胞单层完好性 。
A. muciniphila若何促进粘液厚度尚不清晰。原因之一可能是A. muciniphila通过从降解的粘卵白中造造短链脂肪酸来刺激粘液周转率,那是合成和排泄粘卵白的宿主上皮的优选能源。事实上,A. muciniphila弥补剂增加了小鼠产生粘卵白的杯状细胞的数量。
按捺炎症
有证据表白A. muciniphila能够调理炎症。在加速衰老的小鼠模子中弥补那种细菌能够减轻炎症 。其他研究也显示了A. muciniphila在差别小鼠模子中的抗炎特征,包罗无菌模子、肝损伤模子和瘦削模子。
A. muciniphila能够削减由牙龈卟啉单胞菌引起的瘦或瘦削小鼠的炎症。
此外,A. muciniphila排泄的囊泡可以降低TLR4(Toll-like receptor 4, TLR4)的表达,从而调理NF-κB通路,削减促炎因子IL-6、IL-8的排泄。
调理免疫
A. muciniphila在小鼠体内平衡期间,在诱导肠道驻留 T 细胞方面阐扬着宿主相关的感化。
在一项针对围产期 HIV 传染儿童和青少年的横断面研究中陈述说,A. muciniphila品貌与升高的IL-6 和可溶性 CD14 相关 。
A. muciniphila降解黏卵白,释放能够被四周非黏液降解细菌操纵的短链脂肪酸(SCFAs)、寡糖等代谢物。SCFAs能按捺组卵白脱乙酰基酶,从而调理NF-κB通路,削减炎症因子的表达。丁酸能够促进Treg细胞的外周活化,增加结肠中Treg细胞亚群的数量,按捺促炎免疫细胞CD4+T淋巴细胞、CD8+T淋巴细胞活性。
免疫相关的皮肤病——牛皮癣
银屑病(俗称牛皮癣)是一种免疫介导的慢性炎症性皮肤病。研究表白银屑病和肠道炎症之间存在联系关系。一项研究评估了来自巴西的21名银屑病患者与24名安康对照者的肠道微生物群构成和多样性。与对照组比拟,银屑病患者的 Akkermansia muciniphila 数量有所削减。
扩展阅读:
穿插喂养
除了A. muciniphila外,粘液层中还常见其他微生物。产生丁酸盐的细菌不具有降解粘液的才能,而是操纵被粘卵白降解的物种(如A. muciniphila)降解的碳和氮,那些微生物包罗细菌如Faecalibacterium prausnitzii,罗斯氏菌等其产生抗炎短链脂肪酸(SCFA)。
产生的乙酸可以促进粪厌氧棒状菌(Anaerostipes caccae),霍氏实杆菌(Eubacterium hallii)。
报导共培育A. muciniphila与非粘液降解丁酸盐产生细菌F. prausnitzii、A. caccae和Eubacteriumhallii招致同摄生长和丁酸盐的产生。因而,A. muciniphila不只本身在庇护肠道上皮方面阐扬重要感化,并且还撑持抗炎肠道微生物群。
A. muciniphila和其他细菌之间的彼此感化
Hagi T, et al., Appl Microbiol Biotechnol. 2021有些细菌不克不及降解粘卵白,因而非粘卵白降解细菌受益于粘卵白降解细菌。
A. muciniphila产生来自粘液和短链脂肪酸的糖,如乙酸盐和丙酸盐。非粘液降解细菌,如Anaerostipes caccae, Eubacterium hallii and Faecalibacterium prausnitzii ,操纵A. muciniphila从粘液中降解的糖停止生长。
A. muciniphila的粘卵白降解撑持了Anaerostipes caccae的生长和丁酸消费。Anaerostipes caccae诱导AKK中粘卵白降解基因的表达增加,核糖体基因的表达削减。
避免体重增加
遍及发现A. muciniphila在瘦个别中更为丰硕。在超重个别中,细菌的品貌较低。
在小鼠中,与瘦削小鼠的品貌比拟,瘦动物粪便中A. muciniphila品貌增加之间的相关性表白了那种意义,而且察看到在数周内每天向高脂肪饮食诱导的瘦削小鼠喂食Akkermansia显然能够逆转那种诱导的瘦削以及改善上皮完好性和相关效应。
也有一些数据表白,A. muciniphila干涉可能成为人类受试者瘦削改善计划的根底。但是强调只要活的Akkermansia菌才气在小鼠中产生那种效果,但是发现高温预处置杀菌的细胞以至纯化的Akkermansia卵白,与活细胞治疗的效果比拟,Akkermansia的热杀死细胞似乎对高脂肪饮食瘦削小鼠具有不异以至加强的有益效果。
此外,A. muciniphila通过火解粘卵白产生醋酸盐如许的 SCFAs,对我们的体重产生积极影响。因为乙酸盐能够阻遏我们感应饥饿,从而避免体重增加。
A.muciniphila治疗不会显著改动饮食诱导的瘦削小鼠的肠道微生物构成,但它能够逆转HFD诱导的代谢紊乱,包罗脂肪量量增加、代谢内毒素血症、脂肪组织炎症和胰岛素抵御,那表白它可能用于预防或治疗瘦削和相关的代谢紊乱。
人类肠道微生物群中丰硕的A.muciniphila可预防疾病
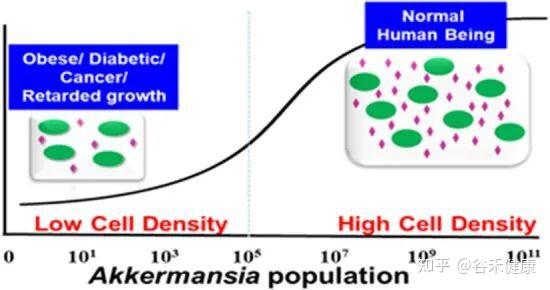 Kalia VC, et al., Indian J Microbiol. 2021
Kalia VC, et al., Indian J Microbiol. 2021改善代谢
A. muciniphila弥补剂可以恢复瘦削和 2 型糖尿病小鼠的粘液厚度,此中高脂肪饮食治疗毁坏了肠道粘液;该治疗还招致血清脂多糖 (LPS) 显着削减,那是一种代谢性内毒素血症,并改善了代谢情况。
对瘦削小鼠施用Akkermansia还通过削减轮回中的炎性脂多糖和减轻胰岛素抵御而招致察看到的“代谢性内毒素血症”削减做为小鼠瘦削的心脏代谢并发症,如动脉硬化。至少来自小鼠模子的结论Akkermansia效应得到了许多差别研究的撑持。
A. muciniphila及其衍消费物对宿主代谢的影响
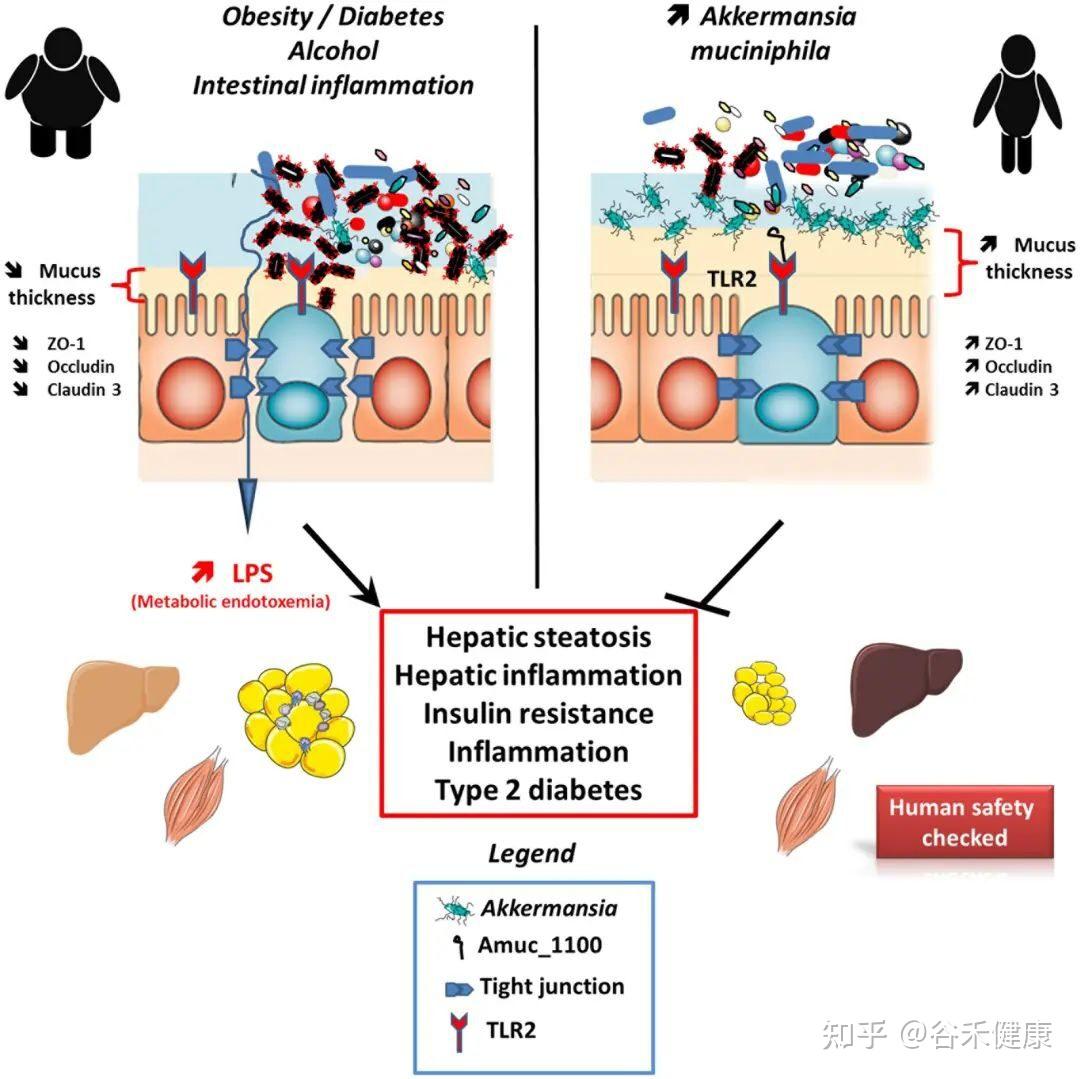 Cani PD,et al.,Front Microbiol. 2017
Cani PD,et al.,Front Microbiol. 2017非酒精性脂肪性肝
与野生型小鼠比拟,在NAFLD小鼠中察看到A. muciniphila品貌显著降低,而招致A.muciniphila品貌增加的干涉办法改善了代谢参数。利用益生元(如低聚果糖)能够恢复A.muciniphila的品貌,并改善相关疾病。
酒精性肝病
酒精性肝病(ALD)由脂肪变性、纤维化和肝硬化开展为急性酒精性脂肪性肝炎,灭亡率高,但治疗办法十分有限。成果发现,内毒素血症程度升高的酒精性肝病患者肝损伤水平增加。乙醇消耗引起的肠道慎密毗连的毁坏招致炎症信号通过病原体相关的分子形式,如脂多糖。
研究ALD患者队列时,发现与安康受试者比拟,ALD患者粪便A. muciniphila数量削减。给乙醇喂养的小鼠口服粘液粘菌A. muciniphila可恢复该细菌的消耗,削减肠漏,增加Claudin-3和Occludin的慎密毗连表达。因而,炎症和肝损伤促进细胞因子白介素1β (IL-1β)和肿瘤坏死因子α (TNF-α)明显削减,招致MPO +中性粒细胞浸润,改善肝损伤。
扩展阅读:
改善血糖和胰岛素抵御
A. muciniphila在糖耐量一般的人群中比糖尿病前期或 II 型糖尿病人群中的数量更多。
事实上,那些细菌已被证明能够加强称为二甲双胍的抗糖尿病药物的感化。在喂食高脂肪饮食的小鼠中,二甲双胍治疗增加了A. muciniphila的数量 并改善了它们的血糖程度。
同样,喂食高脂肪饮食的小鼠口服A. muciniphila但不平用二甲双胍,对葡萄糖的耐受性也有所进步。因而,那种细菌通过改动肠道微生物群,可能有助于在将来找到控造 2 型糖尿病的新办法。
扩展阅读:
癌症免疫治疗
Akkermansia muciniphila也能够积极影响宿主对癌症免疫疗法的反响。研究发现,抗生素的消耗与对免疫治疗 PD-1 阻断剂的反响较差有关。进一步研究确定较低程度的Akkermansia muciniphila确实对反响率有间接影响,给抗生素治疗的小鼠口服细菌弥补剂,发现它恢复了它们对免疫疗法的反响。按照那项研究,有人建议维持安康的肠道菌群,次要包罗Akkermansia muciniphila,关于进步癌症免疫治疗有效性很重要。
此外,Akkermansia muciniphila通过刺激 DCs 产生 IL-12 并促进 CCR9 + CXCR3 + CD4 +的积累来加强 ICB 成效 上皮肿瘤和淋凑趣中的 T 细胞。
按照美国癌症研究中心新研究显示Akkermansia muciniphila提拔免疫查抄点按捺剂的效果,还能产生大量调理T细胞反响的肌苷。食用高纤维食物能够有效地调理肿瘤微情况中的单核巨噬细胞的构成,而食用得越多,Akkermansia muciniphila的肠道菌数量就会更多。
该菌还能产生大量环二腺苷酸,即便是无菌小鼠,仅仅植入Akkermansia muciniphila,它们也能有更强的抗癌反响。将来,或许一种通过食物和环二腺苷酸结合的促进抗癌疗法就在面前。
神经退行性疾病
肌萎缩性侧索硬化症(amyotrophic lateral sclerosis, ALS)是一种复杂的神经退行性疾病,患者凡是会呈现运动神经元的过早灭亡,招致诊断后的均匀保存时间不敷5年。然而,针对肌萎缩性侧索硬化症的药物所做的庞大勤奋却收效甚微。
急性ALS小鼠模子经抗生素治疗后显示,微生物群失调在渐冻症的停顿和恶化中起着重要感化。
通过挑选11株与ALS相关的微生物菌株,包罗A.muciniphila和单接种到经抗生素治疗的ALS小鼠中,只要A.muciniphila与运动神经元改善相关。
其他疾病,例如,帕金森病与对照组的肠道微生物组构成显著差别, Akkermansia 品貌增加。
05
影响Akkermansia muciniphila定植的因素年龄
年龄和天文情况等因素影响人体A. muciniphila的数量。从婴幼儿期间起头A. muciniphila在人类胃肠道定植,并在一年后敏捷接近成年人的程度。跟着年龄增长A. muciniphila在人体内的数量逐步降低。
差别的是,另一研究发现大于60岁人群A. muciniphila的数量升高。此外,别的研究发如今百岁长命白叟中A. muciniphila数量显著增加,提醒A. muciniphila程度的升高可能有助于延缓机体的衰老。
对两品种型的早衰综合征小鼠模子,外用该菌A. muciniphila可显著进步小鼠的安康寿命。
天文位置
别的,差别天文位置A. muciniphila在人群中定植也存在不同。如通细致菌16S rRNA阐发发现,智利安康受试者粪便中的微生物菌群和巴布亚新几内亚受试者有明显差别;但与美国和阿根廷受试者接近;A. muciniphila在智利受试者的丰硕度更高。
中国南方的男性和女性定植率没有差别,但是中国南方人群的A. muciniphila定植率低于欧洲人群。暨南大学理工学院在广州地域人群的A. muciniphila定植率为89.31%,均匀品貌为5.825 lg(CFU/mL)。肠道消化模仿差别时间点的RT PCR成果显示,A. muciniphila在模仿人类肠道微生物菌群情况中具备保存才能;对Bifidobacterium属和Bacteroides属具有按捺效果,对Lactobacillus属具有促进感化。
2021年在Nature颁发的文章中,研究人员将古肠道样本数据和一组来自于已测序的工业化及非工业化生活体例下现代人群的粪便样本数据停止比照。比起非工业化样本和古粪便,包罗Akkermansia muciniphila(可降解人体粘液)在内的BloSSUM类群在工业化样本中更丰硕。
工业化生活下微生物群落中的粘液降解菌和基因更遍及,那可能是由西方饮食招致的。
药物
药物是影响肠道A.muciniphila品貌的重要因素之一。起首,抗菌药物感化后能够间接影响肠道A.muciniphila的数量。
在小鼠出生后早期用万古霉素停止干涉能够有效预防1型糖尿病,显著降低小鼠血糖值以及减轻胰岛炎症;而对8周龄小鼠未见明显预防效果。万古霉素感化于幼儿期间的小鼠使A. muciniphila成为胃肠道优势菌群,该研究提醒A. muciniphila可能是推延1型糖尿病的关键菌群。
对60例6~11个月的婴儿利用阿奇霉素治疗3 d后,婴儿A. muciniphila数量显著削减。此外Dubourg等的研究中,2例成人患者颠末抗生素(强力霉素、哌拉西林、羟氯喹、亚胺培南等)治疗后,A. muciniphila数量显著增加,在肠道菌群的比例均大于40%。
有趣的是,在别的一项小鼠模子中也发现类似现象,给小鼠灌胃四联抗生素(氨苄青霉素,万古霉素,新霉素和甲硝唑)可显著逆转免疫按捺剂招致的A. muciniphila数量削减。那些研究表白抗菌药物等药物利用会影响肠道内A. muciniphila数量的变革,其对人体代谢产生的影响需进一步研究。
最新的研究发现,代谢综合征相关治疗药物对A.muciniphila品貌的影响可能参与其感化机造。如二甲双胍凡是用做治疗代谢综合征(如瘦削和2型糖尿病)的一线用药。
对14例服用二甲双胍的糖尿病患者停止肠道菌群阐发,与未服用二甲双胍的糖尿病患者以及安康受试者比拟,A. muciniphila显著增加。在体外尝试中,搜集二甲双胍治疗组和对照组小鼠的粪便,发现二甲双胍培育组A. muciniphila的比例显著增加。
在别的一项研究利用别的一种代谢病治疗药物利拉鲁肽(Liraglutide)。对高脂饮食诱导的瘦削小鼠停止皮下打针给药,持续15 d给药后处死小鼠,搜集肠道内容物停止菌群阐发,发现治疗小鼠肠道中A. muciniphila显著增加。此外,抗肿瘤药物也能够影响肠道A.muciniphila的品貌。如在胰腺导管腺癌(Pancreatic ductal adenocarcinoma, PDAC)异种移植的小鼠模子中发现,吉西他滨(Gemcitabine)治疗后使A. muciniphila在肠道中的数量显著增加(5%~33%)。
饮食体例
饮食对肠道A.muciniphila影响最显著。
与一般饮食组比拟,高卵白饮食显著降低大鼠肠道A. muciniphila。
Akkermansia 的数量跟着短期(3 周)低FODMAPs饮食而削减。那层见迭出,因为 FODMAP 根本上与益生元纤维不异。
Akkermansia在生酮饮食中显着增加,而且与 Parabacteroides一路,可能是削减酮症癫痫爆发的原因。
小鼠尝试表白,A.muciniphila数量遭到高脂饮食的强烈影响,高脂饮食三周后A.muciniphila品貌起头下降,而且A.muciniphila品貌与体脂呈负相关。
与高脂高糖饮食组比拟,小鼠食用热带生果8周后,能够显著增加A. muciniphila在胃肠道中的品貌;同时干涉后能够降低高脂高蔗糖饮食喂养小鼠的内毒素血症,改善其胰岛素敏感性。
饱和脂肪含量高的饮食与较高的炎症发作率有关。而富含多不饱和脂肪酸的饮食,如亚麻籽和鱼油中的那些,已被证明能够抵御炎症,而且与更瘦的人有关。
那些炊事脂肪也会影响肠道中A. muciniphila的程度。

在一项研究中,老鼠被喂食由差别脂肪构成的差别饮食。一组喂猪油,另一组喂鱼油十一周,成果很有趣。
在鱼油喂养组中,A. muciniphila的品貌增加,乳酸杆菌的品貌也增加。
然后将两组的粪便质料移植到新的小鼠组中,在承受鱼油喂养小鼠粪便移植的小鼠中,它们的A. muciniphila程度增加,炎症程度降低。然而,承受猪油喂养小鼠移植的小鼠的炎症程度很高。
因而,摄入的炊事脂肪类型也会极大地影响肠道中A. muciniphila的数量。
我们已经晓得多酚能够削减炎症并有助于预防许多疾病,因而高多酚食物能够增加Akkermansia.
多酚是强大的抗氧化剂,能够匹敌体内的自在基(与多种疾病有关的化合物,包罗糖尿病、心脏病和癌症)。
有许多差别类型的多酚。此中一些不克不及很好地被身体吸收容在肠道中,那对 Akkermansia来说是个好动静,它们吞噬了多酚并因而加强其力量,从而到达双赢。
此外,丁酸钠和菊粉、北极浆果提取物、绿茶提取物和异麦芽寡糖、炊事多酚等那些益生元也能增加Akkermansia品貌。
06
若何增加Akkermansia muciniphila?含有高程度多酚和鱼油的食物是进步A. muciniphila菌更好的食物。
高多酚食物
多酚使食物一般颜色丰硕多彩,尝起来略带苦味或酸味。泡了很长时间的茶尝起来很苦:浸泡时间越长,茶多酚含量越高。浓橄榄油的青草味或红酒的味道也是很好的例子。

在天然界中,苦味能够抵御想要攻击动物的虫豸。有超越8000种多酚。一些例子是红酒中的白藜芦醇、辣椒中的辣椒素、百里香中的百里酚、肉桂中的肉桂酸、迷迭香中的迷迭香酸。
食物中多酚的含量在很大水平上取决于其生长的土壤、成熟度以及种植、运输和造备体例,因而以下列表仅供参考。
高多酚食物:
蔓越莓、石榴、山莓、黑莓、蓝莓、草莓、樱桃、李子、亚麻种子、黑巧克力、栗子、红茶、绿茶、苹果汁、苹果、黑麦面包、核桃、榛子、红酒。

其他常见的高多酚食物包罗葡萄、橄榄、菠菜、李子和桃子。一般来说,颜色越深越好,所以选择绿色的黑橄榄和葡萄。
油性鱼
Akkermansia 喜好鱼油,但目前还不清晰它们喜好鱼油的特定成分——例如脂肪酸——或者它们喜好所有的部门。所以目前,更好吃鱼。
虽然鱼油如今是有争议的,一些科学家认为它的益处被强调了。研究人员发现,食用整条鲑鱼的一组人的 DHA(一种脂肪酸)程度是食用鱼油的一组人的 9 倍。食用鱼类的同时既增加鱼油,同时增加优良卵白量摄入,均有助于A. muciniphila。
试着每周吃两到三份鱼:
沙丁鱼、鲭鱼、鲱鱼、三文鱼、鳟鱼、鳀鱼、旗鱼、金枪鱼

弥补炊事纤维,选择有机产物。
含纤维的食物:
生菊苣根、绿色蒲公英 、麦麸 、芦笋 、大蒜、香蕉 、洋葱 、韭菜,也存在于燕麦片、红酒、蜂蜜、枫糖浆、豆类和其他食物中。
制止高脂肪饮食和酒精
微生物多样性是我们肠道安康的次要目的。实现那一目的的更佳办法是平衡饮食,吃能让肠道菌群快乐的食物,从而你的觉得也会优良。
益生菌应用难点
A. muciniphila与机体安康联络慎密,有潜力成为新型益生菌。但目前A. muciniphila是专性厌氧菌且难以培育,成为新型益生菌,还有以下几点重要问题亟待处理:
起首,需研发高效快速培育A. muciniphila的新手艺。目前尝试室或小规模已经胜利在尝试室中获得活性A. muciniphila,而且可以不变,但是那只是尝试室规模消费,大规模的工业消费仍是需要处理的问题。好比培育基中存在卵白量来源问题,能否会对人体可能有过敏反响,工业化消费时需研发合理的工业化消费培育基。
其次,需确定平安有效的治疗人群。目前A. Muciniphila 与改善肝功用、降低葡萄糖毒性、减轻氧化应激和按捺炎症有强联系关系,但是,在炎症性肠病、动脉粥样硬化等其他疾病中的干涉,差别研究中存在差别的成果,关于其做为药物面临的平安问题,其应用仍待商榷。
最初,需要优化A. muciniphila的弥补或给药体例。在体外模仿胃肠道的释放尝试中,发现包封的 A. muciniphila活性比间接分离在模仿胃肠道的系统中活性更高,而且可以定向在肠道释放细菌,显著增加A. muciniphila对胃的抵御力,关于实如今肠道的定向给药还需要更多的尝试停止优化。
最初,虽然已经有研究证明有活性的A. muciniphila或者是巴氏消毒的A. muciniphila对人体是平安的,但目前A. muciniphila的临床研究较少,在临床上应用还需要更多的尝试验证。
相关阅读:
次要参考文献
Hasani A, Ebrahimzadeh S, Hemmati F, Khabbaz A, Hasani A, Gholizadeh P. The role of Akkermansia muciniphila in obesity, diabetes and atherosclerosis. J Med Microbiol. 2021 Oct;70(10). doi: 10.1099/jmm.0.001435. PMID: 34623232.
Zhang T, Ji X, Lu G, Zhang F. The potential of Akkermansia muciniphila in inflammatory bowel disease. Appl Microbiol Biotechnol. 2021 Aug;105(14-15):5785-5794. doi: 10.1007/s00253-021-11453-1. Epub 2021 Jul 27. PMID: 34312713.
Druart C, Plovier H, Van Hul M, Brient A, Phipps KR, de Vos WM, Cani PD. Toxicological safety evaluation of pasteurized Akkermansia muciniphila. J Appl Toxicol. 2021 Feb;41(2):276-290. doi: 10.1002/jat.4044. Epub 2020 Jul 28. PMID: 32725676; PMCID: PMC7818173.
Kalia VC, Gong C, Shanmugam R, Lin H, Zhang L, Lee JK. The Emerging Biotherapeutic Agent: Akkermansia. Indian J Microbiol. 2021 Dec 16:1-10. doi: 10.1007/s12088-021-00993-9. Epub ahead of print. PMID: 34931096; PMCID: PMC8674859.
Yu Y, Lu J, Sun L, Lyu X, Chang XY, Mi X, Hu MG, Wu C, Chen X. Akkermansia muciniphila: A potential novel mechanism of nuciferine to improve hyperlipidemia. Biomed Pharmacother. 2021 Jan;133:111014. doi: 10.1016/j.biopha.2020.111014. Epub 2020 Nov 26. PMID: 33246225.
Cheng D, Xie MZ. A review of a potential and promising probiotic candidate-Akkermansia muciniphila. J Appl Microbiol. 2021 Jun;130(6):1813-1822. doi: 10.1111/jam.14911. Epub 2020 Nov 15. PMID: 33113228.
Hagi T, Belzer C. The interaction of Akkermansia muciniphila with host-derived substances, bacteria and diets. Appl Microbiol Biotechnol. 2021;105(12):4833-4841. doi:10.1007/s00253-021-11362-3
Anhê, F. F et al. (2016). Triggering Akkermansia with dietary polyphenols: A new weapon to combat the metabolic syndrome?. Gut microbes, 7(2), 146–153.
Schade L, Mesa D, Faria AR, Santamaria JR, Xavier CA, Ribeiro D, Hajar FN, Azevedo VF. The gut microbiota profile in psoriasis: a Brazilian case-control study. Lett Appl Microbiol. 2021 Dec 12. doi: 10.1111/lam.13630. Epub ahead of print. PMID: 34897759.
Belzer, C et al. (2017). Microbial Metabolic Networks at the Mucus Layer Lead to Diet-Independent Butyrate and Vitamin B12 Production By Intestinal Symbionts. American Society for Microbiology: 8(5).
Caesar, R et al. (2015). Crosstalk Between Gut Microbiota and Dietary Lipids Aggravates WAT Inflammation Through TLR Signalling. Cell Metab: 22(4), pp 658-668.
Dao, M, C et al. (2015). Akkermansia muciniphila and Improved Metabolic Health During a Dietary Intervention in Obesity: Relationship with Gut Microbiome Richness and Ecology. Gut.
de Vos, W, M. (2017). Microbe Profile: Akkermansia muciniphila: A Conserved Intestinal Symbiont that Acts as The Gatekeeper of our Mucosa. Microbiology: 163(5).
Derrien, M et al. (2017). Akkermansia muciniphila and its Role in Regulating Host Functions. Microbial Pathogenesis: 106, pp 171-181.
Everard, A et al. (2013). Cross-Talk Between Akkermansia muciniphila and intestinal Epithelium Controls Diet-Induced Obesity. PNAS: 110(22), pp 9066-9071.
Geerlings, S, Y et al. (2018). Akkermansia muciniphila in the Human Gastrointestinal Tract: When, Where, and How? Microorganisms: 6(3).
Krishnan, A. (2016). Akkermansia muciniphila: What You Need to Know About this Bacterium. uBiome.
Naito, Y et al. (2018). A Next-Generation Beneficial Microbe: Akkermansia muciniphila. J. Clin. Biochem. Nutr: 63(1), pp 33-35.
Ottman, N et al. (2017). Pili-Like Proteins of Akkermansia muciniphila Modulate Host Immune Responses and Gut Barrier Function. PLOS One.
Pierre, J, F et al (2015). Cranberry Proanthocynaidins Improve the Gut Mucous Layer Morpohology and Function in Mice Receiving Elemental Enteral Nutrition. JPEN J Parenter Enteral Nutr: 37(3), pp 401-409.
Shin, N, R et al. (2013). An Increase in the Akkermansia spp. Population Induced by Metformin Treatment Improves Glucose Homeostasis in Diet-Induced Obese Mice. Gut: 63, pp 706-707.
Zhang, T et al. (2019). Akkermansia muciniphila is a promising probiotic. Microbial Biotechnology.
Ouyang J, Lin J, Isnard S, et al. The Bacterium Akkermansia muciniphila: A Sentinel for Gut Permeability and Its Relevance to HIV-Related Inflammation. Front Immunol. 2020;11:645. Published 2020 Apr 9. doi:10.3389/fimmu.2020.00645
Zhou K. Strategies to promote abundance of Akkermansia muciniphila, an emerging probiotics in the gut, evidence from dietary intervention studies. J Funct Foods. 2017;33:194-201. doi:10.1016/j.jff.2017.03.045
Naito, Y., Uchiyama, K. & Takagi, T. A next-generation beneficial microbe: Akkermansia muciniphila. J Clin Biochem Nutr 63, 33–35 (2018).
Derrien, M., Vaughan, E. E., Plugge, C. M. & de Vos, W. M. Akkermansia muciniphila gen. nov., sp. nov., a human intestinal mucin-degrading bacterium. Int. J. Syst. Evol. Microbiol. 54, 1469–1476 (2004).
Hansson, G. C. Role of mucus layers in gut infection and inflammation. Curr. Opin. Microbiol. 15, 57–62 (2012).
van der Lugt, B. et al. Akkermansia muciniphila ameliorates the age-related decline in colonic mucus thickness and attenuates immune activation in accelerated aging Ercc1-/Δ7 mice. Immun. Ageing 16, 6 (2019).
Lukovac, S. et al. Differential modulation by Akkermansia muciniphila and Faecalibacterium prausnitzii of host peripheral lipid metabolism and histone acetylation in mouse gut organoids. MBio 5, (2014).
Dao, M. C. et al. Akkermansia muciniphila and improved metabolic health during a dietary intervention in obesity: relationship with gut microbiome richness and ecology. Gut 65, 426–436 (2016).
Depommier, C. et al. Supplementation with Akkermansia muciniphila in overweight and obese human volunteers: a proof-of-concept exploratory study. Nat. Med. 25, 1096–1103 (2019).
Png, C. W. et al. Mucolytic bacteria with increased prevalence in IBD mucosa augment in vitro utilization of mucin by other bacteria. Am. J. Gastroenterol. 105, 2420–2428 (2010).
Anhê, F. F. et al. A polyphenol-rich cranberry extract protects from diet-induced obesity, insulin resistance and intestinal inflammation in association with increased Akkermansia spp. population in the gut microbiota of mice. Gut 64, 872–883 (2015).
Pierre, J. F. et al. Cranberry proanthocyanidins improve the gut mucous layer morphology and function in mice receiving elemental enteral nutrition. JPEN J Parenter Enteral Nutr 37, 401–409 (2013).
Vinson, J. A. & Cai, Y. Nuts, especially walnuts, have both antioxidant quantity and efficacy and exhibit significant potential health benefits. Food Funct 3, 134–140 (2012).
Mao, B. et al. Effects of different doses of fructooligosaccharides (FOS) on the composition of mice fecal microbiota, especially the bifidobacterium composition. Nutrients 10, (2018).

谷禾安康 是谷禾面向安康范畴的品牌,通过无创收罗微量粪便样品,常温快递运输至谷禾检测中心,经全主动化样品处置和提取后大规模高通量测序获取菌群基因数据并停止阐发解读,凭仗全球领先的样本积累和业界独有的人工智能算法实现了基于肠道菌群的疾病预测和系统安康风险评估, 以及肠道菌群,病原物传染,重金属污染以及营养物量和激素代谢程度等在内的综合安康风险提醒,并供给精准个性化的安康办理计划。公司成立于2012年,总部位于杭州,拥有优良的研发团队和独立尝试室,颠末多年的积累,已完成超12万例临床肠道菌群样本检测,并构建了超37万各类人群样本数据库。
谷禾安康的办事旨在通过持续不竭的研发和改良,大量主动化提拔效率,降低检测成本,为广阔消费者供给更好更有价值的产物。官网:www.guhejk.com
